143 低線量放射線のDNA損傷リスク
掲載日:2025年10月28日
水分解「間接効果」起点に
世界初の評価法
私たちは日々、自然や人工物から放射線を浴びる。放射線による発がんリスクを理解・評価するには、さまざまな過程の科学的知見の蓄積が必要だ。しかし、発がんの出発点「デオキシリボ核酸(DNA)損傷」をすべて実験的に検出するのは非常に困難だ。そのため、計算機シミュレーションによるDNA損傷の形成メカニズム解明や、その生成収量の評価が期待されている。
そこで日本原子力研究開発機構では、低線量放射線がDNAとその周囲にある水分子に与える影響について、シミュレーション解析することに成功。DNA損傷評価法を世界で初めて確立した。
放射線による発がんリスクは200㍉グレイ未満の低線量域では疫学データが少なく、モデルに基づいて推定する。モデルの中には「どんなに低線量でも発がんリスクがある」と考えるもの、その逆で、「ある線量を超えないと発がんリスクは生じない」とするものが存在。現在は前者を採用し、安全性に余裕を持った放射線管理が行われている。
発がんの出発点
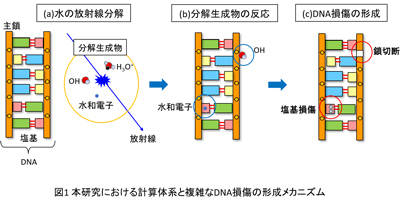
放射線がDNAに当たると損傷が誘発する。対して、放射線が水分子に当たると分解生成物が生じ、DNAに作用して鎖切断や塩基損傷などを引き起こす。前者を放射線の直接効果、後者は間接効果と呼び、DNA損傷に果たす割合は1対3といわれている。
さて、生じたDNA損傷のほとんどは、修復酵素の働きで除去される。ところが、DNA10塩基対(3.4㌨メートル<ナノは10億分の1>)以内に複数個の損傷ができると、DNA損傷の修復効率が低下。発がんの出発点になる。
1放射線の重み
本研究では、計算機シミュレーションで、一つの放射線がDNA近傍の水にヒットした体系を再現。水分解生成物とDNAの化学反応を計算し、放射線影響の起点になる可能性がある、複雑なDNA損傷の形成メカニズムの解明を目指した。
一つの放射線のヒットのみを考慮した、最もシンプルな低線量放射線場といえる設定だ。分解生成物の発生場所とDNAの中心までの距離、分解生成物の種類ごとのDNAとの反応速度などを加味して確率を割り出した。
その結果、複雑なDNA損傷の生成確率はごくわずかながら存在していた。つまり「どんなに低線量でも、ごくわずかながら発がんリスクがある」と考えるモデルを支持することになる。
この知見は放射線防護の新たな基礎概念になると期待できる。今後は、DNA損傷とその修復の関係に展開する予定だ。