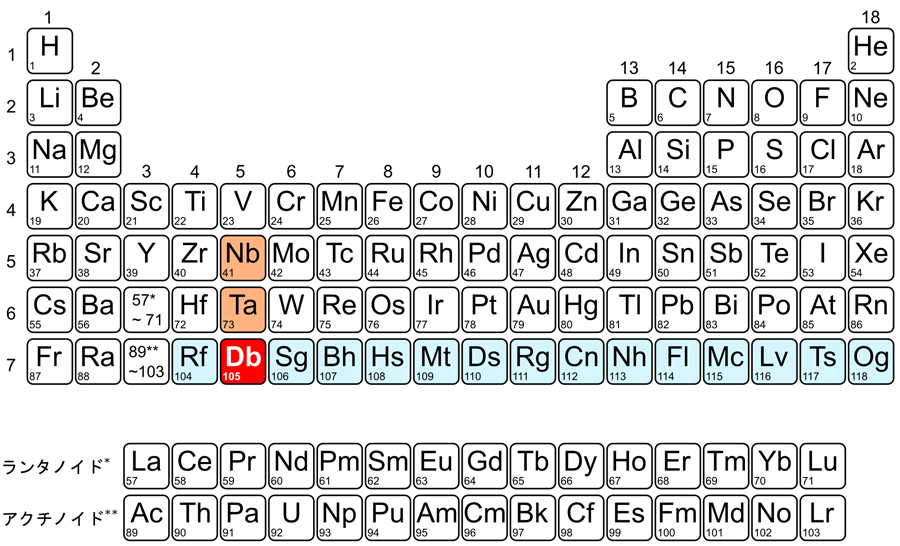令和3年7月7日
国立研究開発法人日本原子力研究開発機構
元素周期表の極限の分子にみつけた周期律のほころび
―超アクチノイド元素ドブニウム化合物の分子の結合に変化が―
【発表のポイント】
- 周期表の極限領域にある重い元素(超重元素)では、周期表の予想から化学的性質がズレる可能性が指摘されてきましたが、超重元素はすべて合成が難しく、寿命の短い人工元素であるため、その実証は困難でした。
- 今回、超重元素のひとつであるドブニウム(Db)に着目し、揮発性を利用した化学分析を試みたところ、純粋な形でのドブニウム化合物の合成・分離にはじめて成功しました。さらにその結果、周期表からの予想と比べ、化合物中でドブニウムが「電子を放出しやすい」という金属的な性質を失っていることがわかりました。
- 本成果によって、105番元素ドブニウム化合物の化学的性質に、「周期表からのずれ」があることが明らかになりました。元素周期表は、周期律という自然界のルールを表現するために約150年前に発明されたものです。今もなお、最適な形が模索されています。今後、周期表の極限領域にある超重元素の化学的性質を解明していくことで、未だ完成されていない周期表全体の理解が進むことが期待されます。
【概要】
国立研究開発法人日本原子力研究開発機構(理事長 児玉敏雄)先端基礎研究センター 重元素核科学研究グループ キエラ・ナディーン博士研究員(現 ポール・シェラー研究所(スイス))、佐藤哲也研究副主幹らは、105番元素「ドブニウム(Db)」の純粋な揮発性化合物の合成と分離に成功し、ドブニウム化合物を形作る化学結合が周期表の予想から変化していることを見出しました。
原子番号が103を超える非常に重い元素は、超アクチノイド元素または超重元素と呼ばれ、大型加速器からの重イオンビームを用いた核融合反応によって人工的に合成されます。このような重い元素では、原子核のまわりを回る電子の運動が光速に近づくことによって、電子の軌道が変化(相対論効果)するために、その化学的性質が周期表の予想からずれてくるのではないかと考えられてきました。
ドブニウムの場合、核反応で合成できる原子の生成率が5分あたり1個程度と極めて低く、そのうえ寿命が約30秒と短いために、一度に一つの原子しか扱うことができません。そのため実験が難しく、発見後50年が経つ今も、その化学的性質はよくわからないままとなっていました。
佐藤研究副主幹らは、原子力機構のタンデム加速器を用いてドブニウムを合成し、独自に開発したオンライン気相化学分離装置によって、ドブニウム揮発性化合物の化学合成と迅速化学分析を試みました。これにより、純粋なドブニウム化合物(オキシ塩化物: DbOCl3)の分離に世界で初めて成功しました。 さらに、周期表からのずれを確かめるために、ドブニウムと同じ周期表第5族元素(遷移金属元素)のニオブ(Nb)やタンタル(Ta)化合物と、揮発性の大きさ(気体になりやすさ)の相互比較を行いました。
比較の結果、周期表からの予想に比べてドブニウム化合物の揮発性が高いことがわかりました。これは、強い相対論効果の影響によって、「電子を放出しやすい」というドブニウムの金属的な性質が薄まり、化合物分子を形成する化学結合が、「電子をお互いに共有する」という非金属的な性質を帯びたためであると考えられます。
相対論効果は、重い元素だけに特有のものではありません。すべての元素に内在します。本成果は、周期表全体への理解につながるだけではなく、近年、物質創生などでますます活用されている理論化学計算の高精度化への貢献が期待されます。
本研究成果は、2021年7月2日にドイツ化学会誌『Angewandte Chemie』(国際版、7月5日号)にオンライン掲載されました(冊子体での発行:8月2日 Vol.60 issue 33)。また、同誌同号の裏表紙に採択されました。
【これまでの背景・経緯】
元素周期表(図1)は化学の分野では地図に等しいものです。周期表がどこまで成り立つのか、あるいはどこかで周期律にほころびが生ずるのかは、化学の基本的な問いのひとつです。原子が原子核と電子から成り立つことはよく知られていますが、原子番号が大きくなるにつれて、原子核の周囲をまわる電子の運動が光の速さに近づくために、 元素の性質を特徴づける電子の軌道が影響を受け(相対論効果)(1)、化学的性質が変化する可能性が以前より指摘されています[1]。このため、元素周期表の重い極限領域にある元素の化学的性質の解明は、興味深いテーマとなっています[2]。
ウランやプルトニウムといったアクチノイドよりもさらに重い原子番号104番以降の元素は、超アクチノイド元素あるいは超重元素と呼ばれています。そのうちのひとつ105番元素ドブニウム(Db)は、米国のギオルソらによって1970年に発見されて以来、もっとも重い第5族元素として元素周期表に配置されています(図1)。しかし、超重元素の合成には特殊な実験設備や、核反応用標的、そして大型の加速器を必要とするために、世界でも実験可能な施設が限られます。さらに、合成できる量も数秒から数時間に1原子と極めて少なく、しかもそのすべてが数分ないし数秒のうちに壊変してしまうため、一度の化学実験にはわずか一個しか取り扱うことができません。このような実験上の困難により、発見後50年が経ってもドブニウムの化学的性質はほとんどわからないままとなっています。
【今回の成果】
今回、ドブニウムの純粋なオキシ塩化物の化学分離に世界で初めて成功しました。さらにその揮発性(気体になりやすさ)を調べたところ、周期表からの予想に比べてドブニウムの揮発性が高いことがわかりました。 このことは、ドブニウム化合物を形作る化学結合において、ドブニウムの金属的な性質(2)が周期表からの予想よりも小さくなっていることに対応します。 本成果は、元素周期表の理解だけではなく、分子設計や物質創生などさまざまな分野で応用が進められている理論計算の高精度化につながることが期待されます。
ドブニウムの化学的性質の検証にあたり、我々はオキシ塩化物に着目しました。ドブニウムと同じ周期表第5族にあるニオブ(Nb)やタンタル(Ta)のオキシ塩化物は、異なる揮発性を持つことが知られています。 これらを相互に比較することができれば、ドブニウムのオキシ塩化物内で起きている「周期表からのずれ」をはっきりさせることができると考えました。
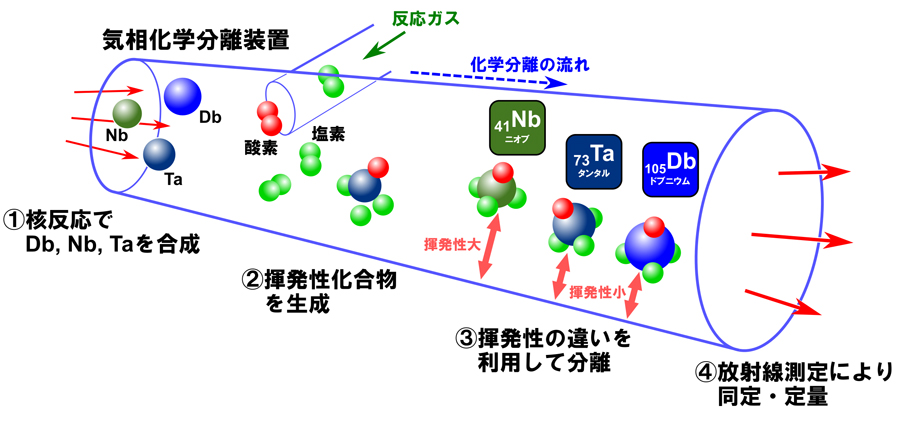
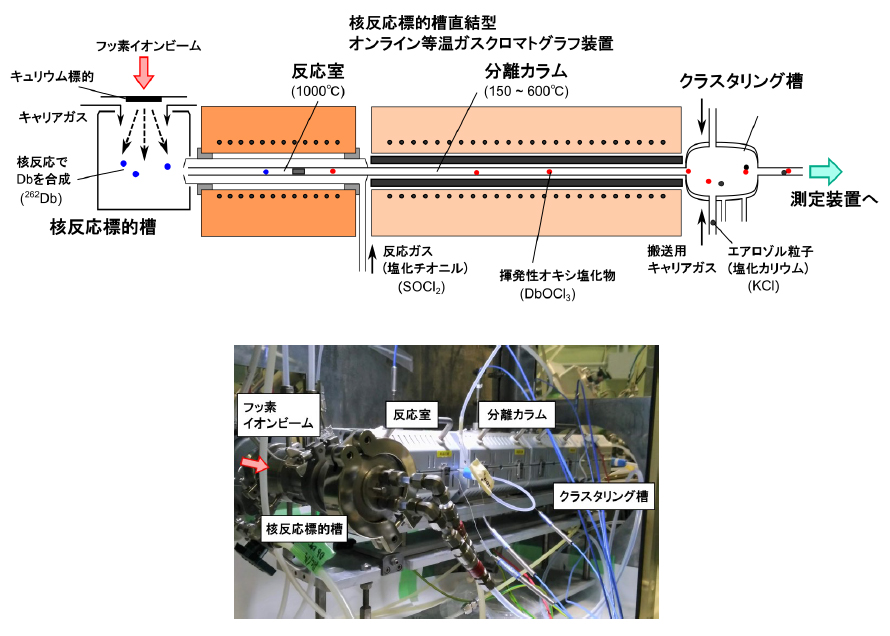
原子力機構タンデム加速器施設(3)を利用して、ドブニウムの揮発性オキシ塩化物の迅速化学合成と、その気相化学分離実験を行いました。実験の概念図を図2に示します。 本実験に用いた核反応標的槽直結型オンライン等温ガスクロマトグラフ装置は、原子力機構にて新たに開発されたものです[3, 4]。 反応室、分離カラム、およびクラスタリング槽から構成されており、タンデム加速器ビームラインに設置された核反応標的槽に直結されています。 実験に用いるドブニウム同位体262Db(半減期34秒)は、タンデム加速器で加速したフッ素(原子番号9)イオンビームをキュリウム(原子番号96)標的に照射して合成しました。 キュリウム標的から飛び出した262Dbは、核反応標的槽内に供給されるキャリアガス中で捕獲され、そのままガス流に乗って反応室へと運ばれます。 1000℃に保たれた反応室には、反応ガスとして微量の酸素を添加した塩化チオニル(SOCl2)蒸気を導入し、迅速にオキシ塩化物の合成を行います。 合成されたオキシ塩化物は、さらに下流の分離カラムへと運ばれます。カラムは石英製であり150℃から600℃までの任意の温度に保つことができます。 カラムに導入された揮発性化合物分子は、カラムの表面とくっついたり離れたりを繰り返して、カラム内を運ばれて行きます。 カラムの温度が十分高ければ、すべての分子がカラムを通り抜けることができますが、温度が低くなるほど通り抜ける効率が小さくなり、最終的に何もカラムから出て来られなくなります。 この変化は化合物の揮発性の高さ(気体になりやすさ)を反映するので、カラム温度の変化に対する目的化合物のカラム通過効率の変化を調べることにより、目的の化合物の揮発性を決定することができます。 カラムを通過した揮発性化合物は、クラスタリング槽で塩化カリウム(KCl)のエアロゾル粒子に捉えられて測定装置へと運ばれ、放射線測定が行われます。 一連の化学分離は5秒程度という極めて短時間で終了します。アルファ壊変(4)する262Dbの検出・同定には、回転円盤型α線測定装置を用いました。 ニオブ(Nb, 原子番号41)およびタンタル(Ta, 原子番号73)の短寿命同位体(88Nb(半減期14.5分)および170Ta(半減期6.8分))についても、フッ素ビームをそれぞれゲルマニウム(原子番号32)およびガドリニウム(原子番号64)標的に照射して合成し、Dbと同様にオキシ塩化物の合成と化学分析を行いました。
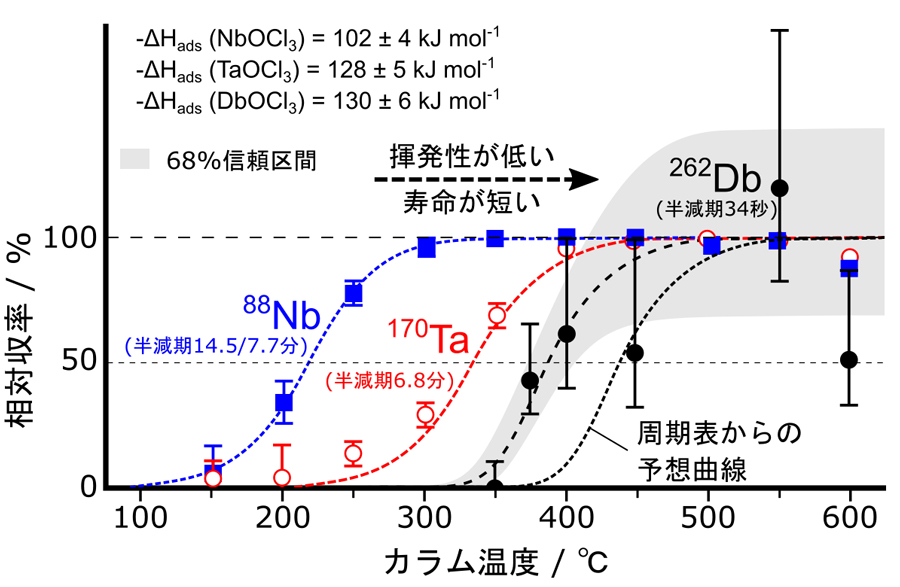
以上の結果、262Dbが壊変する過程で放出されるα線を計24個観測することに成功しました。 262Dbのカラム温度変化に対する収率の変化を、88Nbおよび170Taの収率変化とともに示します(図3)。 過去の報告では、混合物の影響により262Dbの収率変化が広い温度範囲にわたって不定形な推移をしたのに対し、本研究では純物質分離に予想される収量変化が観測されたことから、純粋な262Dbオキシ塩化物が分離されていることを確かめることができました。 さらに、シミュレーションを用いて解析したところ、ドブニウムオキシ塩化物の石英製カラム表面に対する吸着エンタルピー(6)は、ニオブのものよりも大きく、タンタルと同程度でした。吸着エンタルピーが大きいほど、揮発性は低くなります。周期表からは、原子番号の大きなドブニウムは軽い同族元素と比べて電子を放出しやすくなると予想されています。 この場合、分子内の電子の偏りが大きくなるために揮発性はより低くなることが期待されますが、本研究の結果、ドブニウムはニオブよりも明らかに揮発性が低いのに対し、タンタルとほとんど変わらないことが示されました。 このことは、ドブニウムのオキシ塩化物分子を形成する化学結合が、相対論効果によって変化していることを示唆するものであり、ドブニウムが予想よりも金属的な性質を失っていることに対応します。 これは、まさに周期表からの「ずれ」に他なりません。 分子の揮発性には、分子の形状や結合の長さ、分子内の電子の偏りなど、さまざまな要素が関係するため理論計算による予想は困難でしたが、本研究において、ドブニウムのオキシ塩化物の高い揮発性を実験によって与えることができたことにより、理論化学計算へのフィードバックが期待されます。
等温カラム温度を変化させたときの262Dbオキシ塩化物の収率の変化を、88Nbおよび170Taの収率変化と比較して示す。このとき、反応室温度1000℃、オキシ塩素化剤として、毎分200 mLのSOCl2蒸気飽和窒素(1% 酸素)を使用した。一般にカラム温度-収率曲線は、揮発性が低く、寿命が短いほど右に移動する。
得られたカラム温度-収率曲線をモンテカルロシミュレーション(5)を用いて解析することで、オキシ塩化物の等温カラム表面(石英)に対する吸着エンタルピー(-ΔHads)を求めることができた。得られたシミュレーション結果(点線)と-ΔHads値を図中に示す。また、Dbについて周期表から予想される曲線も併せて示した。 この結果、Dbオキシ塩化物は、その吸着エンタルピーがNbよりも大きく、Taと同程度であり、周期表からの予想と比べて高い揮発性を示すことがわかった。
【今後の展望】
相対論効果は、すべての元素に内在するものであり、周期表全体に影響を与えています。本研究成果によって、元素周期表極限領域の元素で顕在化する相対論効果の影響を明らかにしたことにより、周期表全体の理解につながるだけではなく、分子設計などに広く利用される理論化学計算の高精度化に寄与することが期待されます。
【論文情報】
雑誌名:Angewandte Chemie, International Edition, 2021
タイトル:“Chemical Characterization of a Volatile Dubnium Compound, DbOCl3”
著者:Nadine M. Chiera, Tetsuya K. Sato, Robert Eichler, Tomohiro Tomitsuka, Masato Asai, Sadia Adachi, Rugard Dressler, Kentaro Hirose, Hiroki Inoue, Yuta Ito, Ayuna Kashihara, Hiroyuki Makii, Katsuhisa Nishio, Minoru Sakama, Kaori Shirai, Hayato Suzuki, Katsuyuki Tokoi, Kazuaki Tsukada, Eisuke Watanabe, Yuichiro Nagame
DOI:10.1002/anie.202102808
【参考文献】
[1] P. Pyykko, Chem. Rev. 2012, 112, 371-384.
[2] E. Scerri, Sci. Am. 2013, 308, 68-73.
[3] N. M. Chiera, T. K. Sato, T. Tomitsuka, M. Asai, Y. Ito, K. Shirai, H. Suzuki, K. Tokoi, A. Toyoshima, K. Tsukada, Y. Nagame, J. Radioanal. Nucl. Chem. 2019, 320, 633-642.
[4] N. M. Chiera, T. K. Sato, T. Tomitsuka, M. Asai, H. Suzuki, K. Tokoi, A. Toyoshima, K. Tsukada, Y. Nagame, Inorg. Chim. Acta 2019, 486, 361-366.
【用語の説明】
(1) 相対論効果
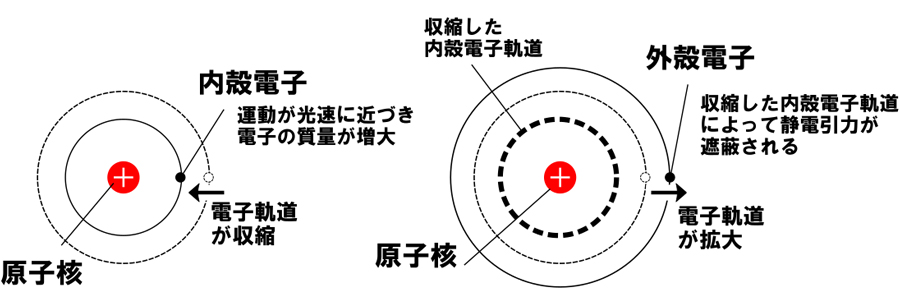
超重元素のような重い原子では、中心にある原子核の正電荷が大きくなるために、負電荷をもつ電子は原子核に強く引き付けられる。その結果、原子核の近くを運動する電子(内殻電子)の速さは光速に近づき、アインシュタインの特殊相対性理論にしたがって電子の質量が増大するために、電子の軌道は収縮する。一方、より外側を運動する電子(外殻電子)では、内殻電子が原子核の正電荷を遮るために、原子核からの静電引力が弱まり、軌道が拡がる。このように電子軌道が影響を受ける現象を相対論効果と呼ぶ。相対論効果はすべての元素に内在しており、原子番号が大きい元素ほど顕著に現れる。特に超重元素では、強い相対論効果の影響によって、化学結合に関わる電子軌道までが変化するために、同族の元素からの予想とは異なる性質を示すことが期待されている。
(2) 金属的な性質
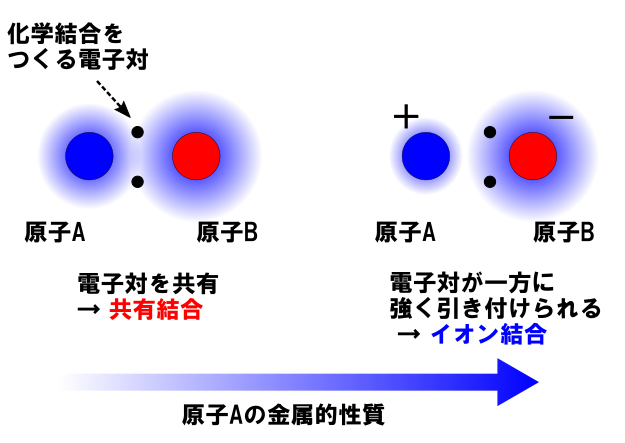
金属は、金属光沢をもち、延性・展性に富むというよく知られる性質の他、化合物を形成する際にも特徴がある。金属原子が非金属原子と結合して分子をつくるとき、一般に金属原子が電子を放出して正電荷を帯びた陽イオンとなり、非金属原子が電子を受け取って負電荷を帯びた陰イオンとなって、正負が引き付けあうイオン結合を形成する。一方、非金属原子同士が分子をつくる場合、電子を共有する共有結合をつくる。
化学結合の模式図を図に示す。図のように、電子対が仲立ちとなることで結合が形成される。電子をお互いに出し合って電子対を共有する結合を共有結合(図左)、電子対が一方に強く引き付けられる場合がイオン結合に対応する(図右)。異なる元素で構成される分子内の化学結合は、このイオン結合と共有結合が混じりあっていると解釈され、電子対が一方に引き付けられる(電荷分布の偏りが大きい)ほど、イオン結合性が強くなる(共有結合性が弱くなる)。イオン結合性が大きいほど金属的な性質が強く、共有結合性が大きいほど金属的な性質が小さいと考えることができる。
電子の放出のしやすさは、同族元素の場合、一般的に原子番号が大きくなるほど(周期表の下に行くほど)大きくなる。しかし、本研究の結果、化合物中において、ドブニウムはタンタルと同程度であることが示唆された。
(3) タンデム加速器【原子力機構原子力科学研究所】
タンデム加速器とは、直流高電圧を利用してイオンを加速する静電加速器の一種であり、加速イオンの電荷を途中で負から正へ変換し、一つの高電圧で2段階加速することで、より高いエネルギーのイオンビームを発生させることができる。タンデム加速器は多様なイオンを加速することが可能であることに加え、エネルギーを正確に制御できることから、精密な原子核物理、物質科学などの研究に広く利用されている。原子力機構原子力科学研究所のタンデム加速器は、現在運用されている世界最大の静電加速器であり、最大1800万ボルトの加速電圧を発生させることができる。これにより、たとえば水素イオンの場合、光速の約27%まで加速することが可能である。原子力機構のタンデム加速器では、上記の特徴の他、核燃料物質やα放射性のアクチノイドなど、特殊な標的を利用できるといった特色を活かした研究が行われている。
(4) アルファ(α)壊変、アルファ(α)粒子
不安定な原子核の放射壊変の1つ。α粒子(ヘリウムの原子核で原子番号2、質量数4)を放出してより安定な原子核に壊変する。この壊変の結果、原子番号が2、質量数が4小さい原子核に変化する。核種に固有なα粒子のエネルギーを測定することによって、262Dbを検出・同定することができる。
(5) モンテカルロシミュレーション
モンテカルロシミュレーションとは、ある現象を記述するモデルがランダムな過程を含むときに、コンピュータ上で発生させた乱数を入力して仮想的な模擬実験を何度も繰り返すことで、近似解を求める計算手法。超重元素のガスクロマトグラフ実験の解析において、カラム内を移動する気体分子や原子の様子をシミュレーションすることにより、カラム表面に対する吸着エンタルピーを見積もることができる。
(6) 吸着エンタルピー
気体状態の分子や原子がある物質表面に吸着する際に生じるエネルギー変化。通常、1モル(mol)当たりのエネルギー変化である[kJ/mol]を単位として表す。吸着エンタルピーが大きいほど、物質表面への吸着の強さが大きい。ガスクロマトグラフ実験等で取得される物理量であり、化合物や原子の揮発性の度合いに対応する。一般に、不活性な表面に対する吸着エンタルピーが大きいほど、揮発性は小さい(気体になりにくい)。