【研究開発の背景と目的】
植物の色素成分であるアントシアニンやフラボノール7)は、色素の原料となる分子に糖が付加された化合物です。Ct3GT-Aは、この糖の付加反応を担っています。これらの物質は、優れた生理活性を示すことでも知られており、食品から医薬品に至るまで幅広い分野で利用されています。また、この糖付加反応を利用すれば、有機低分子の化学的および生物学的性質を変えることが可能です。たとえば、水に溶けにくく医薬品として利用できなかった生理活性物質は、糖の付加によって可溶性や安定性が高まり、医薬品候補物質としての利用が可能となります。
植物体における糖の付加は、Ct3GT-Aなど糖転移酵素8)によって生じます。糖転移酵素は、糖ヌクレオチド9)から色素の原料となる分子の水酸基やアミノ基、カルボキシル基などに糖を転移する反応を触媒します。近年、チョウマメ(図1A)に特徴的なアントシアニン色素であるテルナチンの生合成に関わる糖転移酵素として、Ct3GT-A、Ct3GT-BおよびCt3′5′GTが見出されました(図1B)。Ct3GT-BおよびCt3′5′GTは、Ct3GT-Aに対して極めて高いアミノ酸配列の相同性を示す類縁タンパク質であり(Ct3GT-B:92%の配列が一致、Ct3′5′GT:87%の配列が一致)、色素原料の活性化(脱プロトン化10))に必須のアミノ酸残基(触媒残基)をともに保持しています。しかしながら、その色素原料の選択性には大きな違いがあり、Ct3GT-Aの立体構造を知ることは、類縁のCt3GT-BおよびCt3′5′GTの選択性の違いを理解することにも繋がります。
そこで本研究では、アントシアニジンに対して高い糖転移活性を示すCt3GT-Aの立体構造を決定すると共に、色素原料との結合部位についての構造情報の取得を試みました。
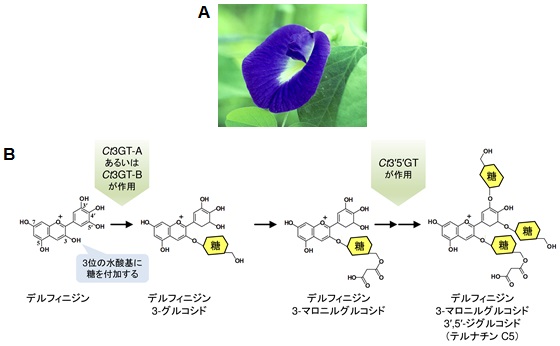
図1 (A)チョウマメの花 (B)チョウマメの花色素テルナチンの生合成経路
【研究の手法と成果】
チョウマメの花弁に含まれるCt3GT-Aは、デルフィニジンなどのアントシアニジンに対して高い糖転移活性を示す酵素です(図2)。これまで、水溶液中で不安定なアントシアニジンが結合した酵素-基質複合体の立体構造は報告されていませんでした。水溶液中での不安定さは、アントシアニジンの1位11)の酸素原子がプラスの電荷を持つためと考えられます。そこで本研究では、2種類のアントシアニジン、デルフィニジンあるいはペチュニジンを有機溶媒に溶解した後、速やかにタンパク質結晶を含む水溶液中に添加すること、またスクリーニングにより見出した弱酸性の結晶化条件を用いることで、デルフィニジン複合体とペチュニジン複合体の立体構造の決定に成功しました(図3A、3B、3C)。これは、酵素に結合した状態で、プラスの電荷を帯びたアントシアニジンの分子構造を世界で初めて明らかにした例になります。
一方、フラボノールの一種で、アントシアニジンとは発色の異なるケンフェロールに対する糖転移活性は、デルフィニジンに比べて約20倍も低いことが分かりました。フラボノールに特徴的な4位のカルボニル基が、Ct3GT-Aへの結合の障害になるためと考えられます(図2)。そこでケンフェロールとの複合体の立体構造を決定し(図3D)、両者の結合した状態を比較してみましたが、その結果は予想とは異なり、デルフィニジンとケンフェロールの結合様式に大きな違いは見られませんでした。
一般に、基質と酵素の関係は「鍵」と「鍵穴」の関係に例えられ、酵素(Ct3GT-A)は基質となる分子(アントシアニジンやフラボノール)の構造の違いを見分けていると考えられています。しかしながら、本解析の結果、Ct3GT-Aはアントシアニジンとフラボノールの構造の違いを識別しているのではなく、むしろ両者に共通の構造を認識していることが分かりました。このことから、異なる糖転移活性を示す理由の一つとして、糖が付加される3位水酸基の脱プロトン化のしやすさが影響していると考えられます。実際、プラスの電荷を帯びたアントシアニジンの3位水酸基はフラボノールよりも脱プロトン化しやすいことが、計算科学的手法に基づき提案されています。以上の知見から、Ct3GT-Aの基質認識は酵素としてはむしろ寛容であり、様々な低分子化合物への糖の付加を可能とする人工酵素をデザインする上で、有用な土台になると期待されます。
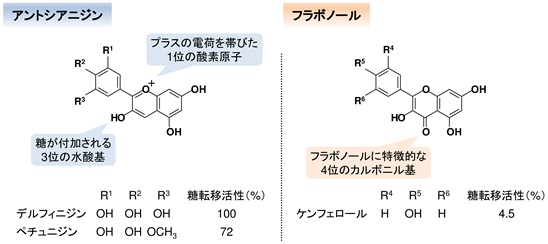
図2 色素原料の化学構造と糖転移活性
単環上の置換基の種類と数により、それぞれ異なる色調を発現する。糖転移活性は、デルフィニジンに対する相対値を示している。
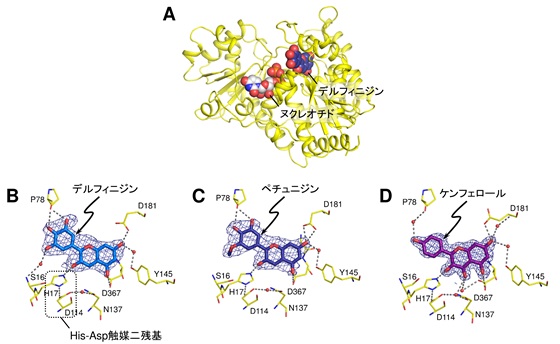
図3 Ct3GT-Aの立体構造と色素原料結合部位
(A)タンパク質部分(黄色)に糖ヌクレオチドの一部(炭素原子を白色)とアントシアニジンの一種、デルフィニジン(炭素原子を濃紺)が結合している様子を示す。また、デルフィニジン複合体(B)、ペチュニジン複合体(C)、ケンフェロール複合体(D)の各色素原料結合部位の拡大図を示す。色素原料を囲んでいる網(紺色)は、本解析により得られた“電子密度”を示している。それぞれ異なる糖転移活性を示すにもかかわらず、糖が付加される3位の水酸基は、His-Asp触媒二残基12)と同様に相互作用している。
【今後の期待】
本研究成果のポイントは、放射光を利用したX線結晶構造解析により、水溶液中で不安定なアントシアニジン(デルフィニジンおよびペチュニジン)が酵素に結合した様子を世界に先駆けて明らかにしたことです。また、糖転移活性の異なるアントシアニジンおよびフラボノールが同じ様式で結合していたことから、Ct3GT-Aによるアントシアニジン選択的な糖転移反応が、同分子の脱プロトン化しやすい性質に由来することが示されました。
今後、異なる色素原料を基質とする類縁タンパク質との構造比較により、その選択性の改変に必要な結合部位の人工的デザインが可能になります。つまり、目的とする糖転移活性を有する組換えタンパク質13)の作製により、発色の異なる色素の合成、あるいは本色素原料を基にした医薬品候補物質の開発が可能となります。また、組換えタンパク質を植物体内で機能させることにより、花の色など植物体の色を改変する技術の開発にも繋がると期待されます。